کامل ترین جدول تناوبی تا به امروز
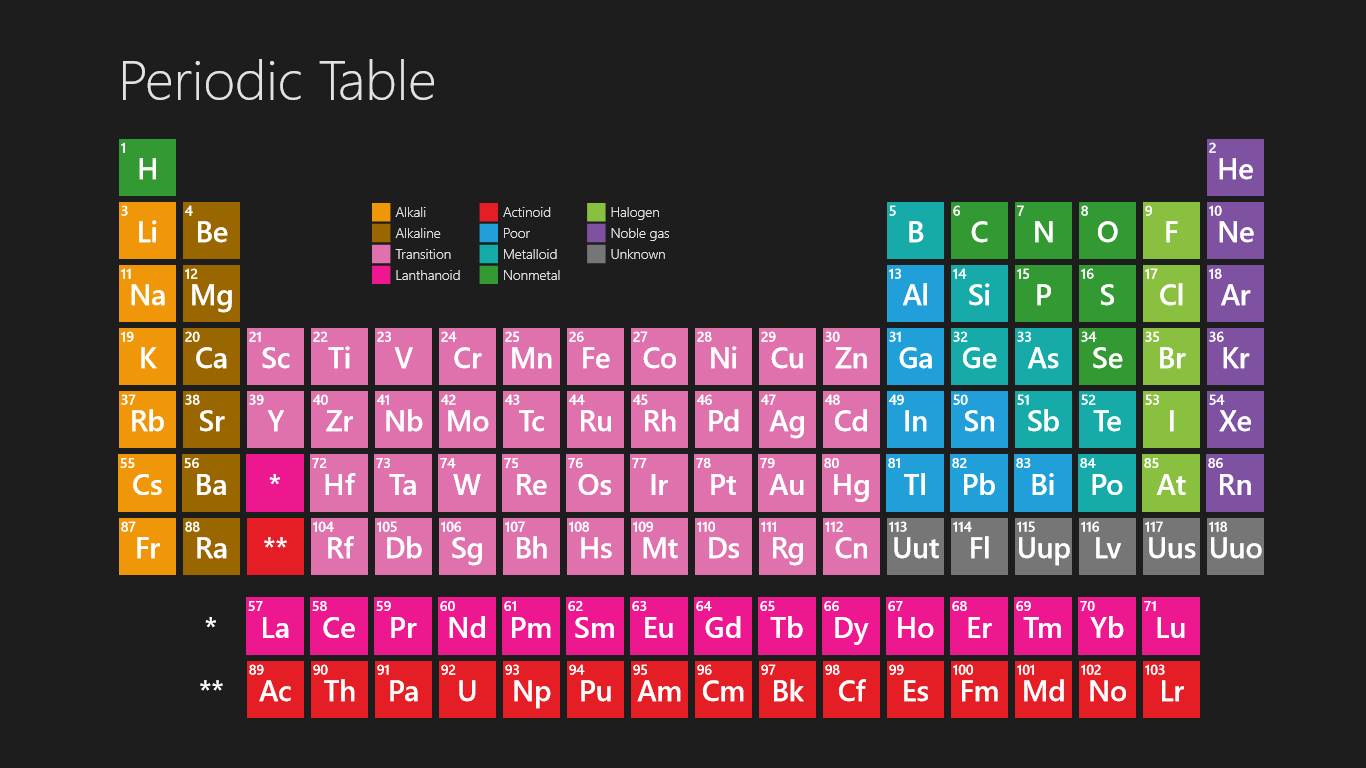
لینک دانلود در ادامه ی مطلب
همانطوری که می دانید شیمی درسی است که برای رشته علوم تجربی بسیار مهم است و باید بر روی آن تمرکز کنید تا به خوبی مطالب آن را بیاموزید و در ذهن خود ثبت کنید.پس باید نمونه سوالات زیادی را حل کنید تا نمرات خوبی را به دست بیاورید.لینک دانلود در ادامه ی مطلب
نمونه سئوال فصل اول شیمی یازدهم – کانون فرهنگی آموزش (قلمچی)
نمونه سئوال فصل اول شیمی یازدهم – گروه آموزشی جوکار (گاج)
نمونه سوال گرما شیمی – فصل دوم
مسائل درصد خلوص به سه بخش تقسیم میشن:
بخش اول : در این نوع مسائل جرم ماده ی خالص همراه با درصد خلوص آن داده می شود و جرم ماده ی دیگری از معادله ی شیمیایی خواسته می شود . در این صورت ابتدا جرم ماده خالص را بدست آورده و سپس وارد مساول استوکیومتری می کنیم .
درصد خلوص برابر است باجرم ماده ی خالص(گرم) بر جرم ماده ی ناخالص(گرم) ضرب در 100
مثال:۵۰ گرم آلومینیوم کلرید با درصد خلوص ۸۰٪ در واکنش با سود سوزآور چند گرم آلومینیوم هیدروکسید ایجاد می کند ؟
*اولین کاری که میکنیم می بین معادله موازنه شده هست یا نه اگه موازنه بود که به بقیه ی کارمون ادامه میدیم در غیر این صورت باید معادله را با روش وارسی یا هر روش دیگه ایی که بلد هستین موازنه کنید.
AlCl3 + 3 NaOH __________> 3NaCl + Al ( OH )3
%80 =( g AlCl3 ÷ 50) × 100 __________> AlCl3 = 40g
? g Al ( OH )3 = 40g AlCl3× 1 mol AlCl3 / 133/5 g AlCl3× 1mol Al ( OH )3 / 1mol AlCl3 × 78 g Al ( OH )3 / 1mol Al ( OH )3 = 23/37 g Al ( OH )3
بخش دوم : در این نوع مسائل مقدار ماده ناخالص را می خواهند و درصد خلوص آن را می دهند . در این صورت از روابط استوکیومتری مقدار ماده ی خالص را پیدا کرده و یا در فرمول درصد خلوص قرار داده و جرم ماده ی ناخالص را پیدا می کنیم یا آخرین عددی که از روابط استوکیومتری یدست می اید در معکوس درصد خلوص ضرب می کنیم .
مثال:برای تهیه ی ۴۰ گرم هیدروژن از واکنش آلومینیوم با HCl چند گرم پودر آلومینیوم با درصد خلوص ۸۵٪ نیاز است ؟
2Al + 6HCl __________> 2AlCl3 + 3H2
? g Al = 40g H2 × 1 mol H2 / 2gH2 × 2 mol Al / 3 mol H2 × 27 gAl / 1 mol Al × 100 / 85 = 423/5 g Al
بخش سوم : در این نوع مسائل مقدار ماده ی ناخالصرا می دهند . معولاْ این عدد را وارد روابط استوکیومتری نمی کنیم . آن را کنار گذاشته و با استفاده از روابط استوکیومتری مقدار ماده ی خالص را به وسیله ی داده های دیگر مسئله حساب کرده و سپس در فرمول درصد خلوص گذاشته و مقدار ماده ی خواسته شده را محاسبه می کنیم .
مثال: از واکنش ۱۲۰ گرم کلسیم کربید ناخالص در آب ۳۹ گرم گاز استیلن حاصل شده است . تعیین کنید درصد خلوص کلسیم کربید چقدر است ؟
CaC2 + 2H2O __________> Ca (OH)2 + C2H2
? g CaC2= 39 g C2H2× 1mol C2H2/26g C2H2 ×1mol CaC2/ 1mol C2H2 = 96g CaC2 «مقدار خالص»
(۹۶÷۱۲۰) × 100 = ۸۰٪ =درصد خلوص
 به همین راحتی که دیدین
به همین راحتی که دیدین
دسته ی اول: مسائلی که در آن ها، مقدار عملی داده می شود و بازده ی درصدی مورد سوال است. در این گونه از مسائل، با توجه به مقدار واکنش دهنده ( اگر دو واکنش دهنده وجود داشته باشد، واکنش دهنده ی محدود کننده در نظر گرفته می شود. ) مقدار نظری تولید همان فراورده را با همان یکا محاسبه می شود و با توجه به رابطه بازده ی درصدی واکنش به دست خواهد آمد.
دسته ی دوم: مسائلی که در آن ها، بازده ی درصدی داده می شود و مقدار عملی باید محاسبه شود. در این صورت با توجه به روابط استوکیومتری، مقدار نظری فراورده ی مورد نظر محاسبه می شود و با توجه به رابطه ی بازده ی درصدی مقدار مجهول محاسبه می شود.
دسته ی سوم: مسائلی که در آن ها هم مقدار عملی و هم بازده ی درصدی داده می شود که در این صورت مقدار واکنش دهنده مورد سؤال است. در این گونه مسائل، با استفاده از بازده ی درصدی، مقدار نظری محاسبه می شود، در پایان با توجه به مقدار نظری فراورده های مورد نظر، مقدار واکنش دهنده ی لازم محاسبه می شود.
بازده دصدی برابر است با مقدار عمل فراورده بر مقدار نظری فراورده ضرب در 100